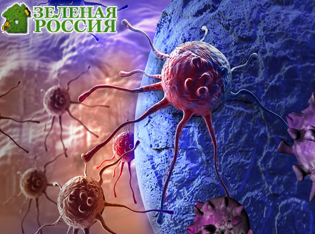
Учёные из Медицинского центра UT Southwestern обнаружили два липида, которые совместно с ключевым белком иммунной системы — STING (стимулятором генов интерферона) — запускают иммунный ответ в организме. Результаты исследования, опубликованные сразу в двух статьях журнала Nature, могут привести к созданию новых методов управления иммунитетом для борьбы с инфекциями, онкологическими и аутоиммунными заболеваниями, а также нейродегенеративными расстройствами.
Исследователи показали, что сигнальный путь cGAS-STING имеет более сложную систему регуляции, чем считалось ранее. Контроль активности этого механизма крайне важен: он позволяет организму эффективно реагировать на инфекции и одновременно предотвращать атаки иммунной системы на собственные ткани. Нарушения работы этого пути уже связывают с рядом воспалительных и аутоиммунных болезней.
Одним из авторов работ стал профессор молекулярной биологии Чжицзянь «Джеймс» Чен — один из ведущих мировых специалистов по врождённому иммунитету. Ранее он открыл фермент cGAS, который производит молекулу cGAMP — ключевой сигнал, активирующий STING. Это открытие принесло ему ряд престижных наград, включая Japan Prize 2026, премию Альберта Ласкера и Breakthrough Prize.
Как работает система STINGSTING — важнейший элемент врождённого иммунитета, который обеспечивает быструю защиту от вирусов, бактерий, грибков, паразитов и опухолевых клеток. Одним из сигналов для активации служит чужеродная ДНК, появляющаяся в цитоплазме клетки. Фермент cGAS распознаёт такую ДНК и запускает синтез cGAMP, который связывается со STING.
В неактивном состоянии STING находится в эндоплазматическом ретикулуме. После связывания с cGAMP белки STING активируются, объединяются в цепочки (олигомеризуются) и перемещаются в аппарат Гольджи, где запускают каскад сигналов, формирующий иммунный ответ.
Долгое время оставалось непонятно, как именно происходит объединение STING и почему его перемещение между клеточными структурами так важно.
Роль липида PtdIns(3,5)P2 и холестеринаКоманда под руководством Джеймса Чена исследовала молекулы, взаимодействующие со STING, и обнаружила ключевой фермент PIKfyve, который производит липид PtdIns(3,5)P2. Когда учёные удаляли PIKfyve из клеток, STING переставал перемещаться в аппарат Гольджи и не запускал иммунный сигнал.
Эксперименты показали, что липид PtdIns(3,5)P2 напрямую связывается со STING и усиливает его активацию молекулой cGAMP. Это означает, что липид действует совместно с основным сигналом и является необходимым элементом включения иммунного механизма.
Параллельно другая группа исследователей подтвердила, что именно PtdIns(3,5)P2 необходим для формирования цепочек STING. Используя крио-электронную микроскопию, учёные увидели, что этот липид располагается между молекулами STING и выполняет роль «моста», соединяющего их.
Неожиданно рядом с местом связывания обнаружили молекулы холестерина. Оказалось, что холестерин стабилизирует линейную структуру STING и помогает формировать устойчивые цепочки.
Почему STING должен перемещаться внутри клеткиПолученные результаты объяснили, почему STING перемещается из эндоплазматического ретикулума в аппарат Гольджи. В ретикулуме концентрация PtdIns(3,5)P2 и холестерина относительно низкая, тогда как в аппарате Гольджи и связанных с ним пузырьках она значительно выше. Именно это создаёт условия для формирования длинных цепочек STING и запуска иммунного ответа.
Дополнительные эксперименты с мутациями показали: если нарушить участки STING, связывающиеся с липидом и холестерином, белок перестаёт формировать цепочки и не запускает сигнальный каскад. Это подтвердило ключевую роль обнаруженных молекул.
Значение открытия для медициныИсследование имеет не только фундаментальное значение, но и практическое. Понимание того, какие молекулы активируют STING и как происходит их взаимодействие, позволяет создавать лекарства, которые могут усиливать или подавлять этот механизм.
Активация STING потенциально поможет организму эффективнее бороться с инфекциями и опухолями. Напротив, подавление его активности может стать стратегией лечения аутоиммунных и нейродегенеративных заболеваний.
Учёные планируют продолжить изучение пути cGAS-STING, чтобы использовать эти знания для разработки новых терапевтических подходов. По их мнению, управление этим механизмом может стать одним из ключевых направлений медицины будущего, позволяя точечно регулировать иммунный ответ в зависимости от заболевания.




 Учёные из Медицинского центра UT Southwestern обнаружили два липида, которые совместно с ключевым белком иммунной системы — STING (стимулятором генов интерферона) — запускают иммунный ответ в организме. Результаты исследования, опубликованные сразу в двух статьях журнала Nature, могут привести к созданию новых методов управления иммунитетом для борьбы с инфекциями, онкологическими и аутоиммунными заболеваниями, а также нейродегенеративными расстройствами.
Учёные из Медицинского центра UT Southwestern обнаружили два липида, которые совместно с ключевым белком иммунной системы — STING (стимулятором генов интерферона) — запускают иммунный ответ в организме. Результаты исследования, опубликованные сразу в двух статьях журнала Nature, могут привести к созданию новых методов управления иммунитетом для борьбы с инфекциями, онкологическими и аутоиммунными заболеваниями, а также нейродегенеративными расстройствами.


 Арахисовое масло с пониженным содержанием жираКогда производители исключают один ингредиент, они, как правило, чтобы наверстать упущенное ...
Арахисовое масло с пониженным содержанием жираКогда производители исключают один ингредиент, они, как правило, чтобы наверстать упущенное ... Новое исследование, опубликованное в журнале Nature Ecologyand Evolution, показало, что самые крупные животные не имеют пропорционально ...
Новое исследование, опубликованное в журнале Nature Ecologyand Evolution, показало, что самые крупные животные не имеют пропорционально ... Желтые зубы является одной из тех стоматологических проблем, которая возникает у многих взрослых людей. Зубы человека не могут быть от ...
Желтые зубы является одной из тех стоматологических проблем, которая возникает у многих взрослых людей. Зубы человека не могут быть от ...